विषय
प्रतिशत द्रव्यमान एक रासायनिक यौगिक बनाने वाले प्रत्येक तत्व का प्रतिशत निर्धारित करता है। इस मान को खोजने के लिए, आपको घोल / मोल्स में यौगिक तत्वों के मोलर द्रव्यमान या समाधान बनाने के लिए उपयोग किए गए ग्राम की संख्या की आवश्यकता होगी। प्रतिशत द्रव्यमान की गणना एक मूल सूत्र का उपयोग करके सरल तरीके से की जा सकती है जो यौगिक (या समाधान) के द्रव्यमान से तत्व (या विलेय) के द्रव्यमान को विभाजित करता है।
कदम
2 की विधि 1: दिए गए द्रव्यमान के साथ प्रतिशत द्रव्यमान ज्ञात करना
- एक यौगिक के प्रतिशत द्रव्यमान के लिए समीकरण को परिभाषित करें। एक यौगिक का मूल सूत्र है: प्रतिशत द्रव्यमान = () x 100. आपको मानों को प्रतिशत के रूप में व्यक्त करने के लिए परिणाम को 100 से अंत में गुणा करना होगा।
- एक रासायनिक यौगिक का द्रव्यमान जिसमें आप रुचि रखते हैं समस्या में दिया गया द्रव्यमान है। यदि यह मान प्रदान नहीं किया गया है, तो निम्न विधि का संदर्भ लें और सीखें कि जब द्रव्यमान नहीं दिया जाता है तो प्रतिशत द्रव्यमान कैसे प्राप्त करें।
- एक यौगिक के कुल द्रव्यमान की गणना यौगिक या समाधान बनाने के लिए उपयोग किए गए सभी तत्वों के द्रव्यमान को जोड़कर की जाती है।
यौगिक के कुल द्रव्यमान की गणना करें। जब आप सभी तत्वों या यौगिकों के द्रव्यमान का मूल्य जानते हैं, तो आपको केवल यौगिक के द्रव्यमान या अंतिम समाधान की गणना करने के लिए उन्हें जोड़ना होगा। यह मान प्रतिशत द्रव्यमान की गणना में भाजक होगा।- उदाहरण के लिए: 100 ग्राम पानी में 5 ग्राम सोडियम हाइड्रॉक्साइड का प्रतिशत द्रव्यमान क्या है?
- यौगिक का कुल द्रव्यमान सोडियम पेरोक्साइड की मात्रा प्लस पानी की मात्रा है: 100 ग्राम + 5 ग्राम, कुल 105 ग्राम का द्रव्यमान।

विचाराधीन रसायन के द्रव्यमान को पहचानें। जब आप को खोजने की जरूरत है प्रतिशत द्रव्यमान, समस्या यह है कि आप सभी तत्वों के कुल द्रव्यमान के प्रतिशत के रूप में एक विशिष्ट तत्व (प्रश्न में तत्व) के द्रव्यमान का पता लगाना चाहते हैं। प्रश्न में तत्व के द्रव्यमान पर ध्यान दें। यह मान प्रतिशत द्रव्यमान की गणना में अंश होगा।- उदाहरण के लिए, तत्व का द्रव्यमान सोडियम हाइड्रोक्साइड का 5 ग्राम है।
- प्रतिशत द्रव्यमान सूत्र में चर को प्रतिस्थापित करें। प्रत्येक चर के लिए मान निर्धारित करने के बाद, उन्हें समीकरण में बदलें।
- उदाहरण के लिए: प्रतिशत द्रव्यमान = () x 100 = () x 100।

प्रतिशत द्रव्यमान की गणना करें। अब जब समीकरण बनता है, तो इसे हल करें ताकि प्रतिशत द्रव्यमान की गणना की जा सके। यौगिक के कुल द्रव्यमान से तत्व के द्रव्यमान को विभाजित करें और 100 से गुणा करें। परिणाम रासायनिक तत्व का प्रतिशत द्रव्यमान होगा।- उदाहरण के लिए: () x 100 = 0.04761 x 100 = 4.751%। इस प्रकार, 100 ग्राम पानी में 5 ग्राम सोडियम हाइड्रॉक्साइड का प्रतिशत द्रव्यमान 4.751% है।
विधि 2 की 2: द्रव्यमान के साथ प्रतिशत द्रव्यमान ज्ञात नहीं है
- एक यौगिक के प्रतिशत द्रव्यमान के लिए समीकरण को परिभाषित करें। किसी यौगिक के प्रतिशत द्रव्यमान का मूल सूत्र है: प्रतिशत द्रव्यमान = () x 100. आपको मानों को प्रतिशत के रूप में व्यक्त करने के लिए अंत में परिणाम को 100 से गुणा करना होगा।
- जब आप बड़े पैमाने पर मूल्यों को नहीं जानते हैं, तो आप मोलर द्रव्यमान का उपयोग करके यौगिक के एक तत्व का प्रतिशत द्रव्यमान पा सकते हैं।
- उदाहरण के लिए: पानी के अणु में हाइड्रोजन का प्रतिशत द्रव्यमान कितना है?.
लिखना रासायनिक सूत्र. यदि प्रत्येक यौगिक के लिए रासायनिक सूत्र प्रदान नहीं किए गए हैं, तो आपको उन्हें लिखना होगा। अन्यथा, चरण पर जाएं "प्रत्येक तत्व का द्रव्यमान ढूंढें"।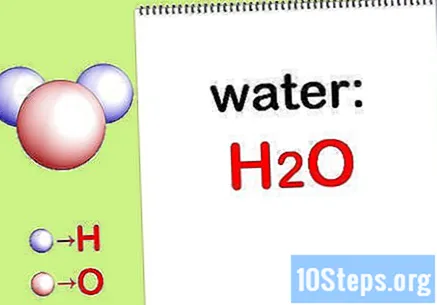
- उदाहरण के लिए, पानी के लिए रासायनिक सूत्र लिखें: एच2द।
यौगिक में प्रत्येक तत्व का द्रव्यमान ज्ञात कीजिए। आवर्त सारणी का हवाला देकर रासायनिक सूत्रों के प्रत्येक तत्व के आणविक भार को देखें। आम तौर पर, एक तत्व का द्रव्यमान रासायनिक तत्व प्रतीक के नीचे पाया जा सकता है। यौगिक के प्रत्येक तत्व के द्रव्यमान पर ध्यान दें।
- उदाहरण के लिए, ऑक्सीजन का आणविक द्रव्यमान 15.9994 है, और यह हाइड्रोजन 1.0079 है।
दाढ़ अनुपात से द्रव्यमान को गुणा करें। पहचानें कि रासायनिक तत्व में प्रत्येक तत्व के कितने मोल हैं। कंप की सब्सक्राइब्ड संख्या द्वारा मोल्स की संख्या दी गई है। दाढ़ अनुपात द्वारा प्रत्येक तत्व के आणविक द्रव्यमान को गुणा करें।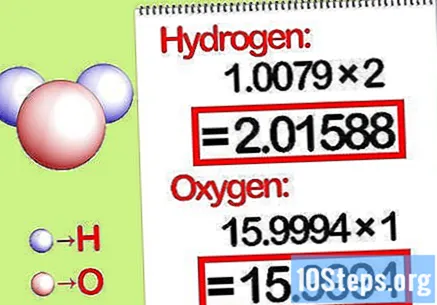
- उदाहरण के लिए, पानी में ऑक्सीजन से हाइड्रोजन का दाढ़ अनुपात 2: 1 है। इसलिए, हाइड्रोजन के आणविक भार को दो (1.00794 X 2 = 2.01588) से गुणा करें और ऑक्सीजन के आणविक भार को छोड़ दें क्योंकि यह (15.9994) है।
यौगिक के कुल द्रव्यमान की गणना करें। यौगिक के सभी तत्वों का कुल द्रव्यमान जोड़ें। दाढ़ अनुपात द्वारा गणना किए गए द्रव्यमान का उपयोग करना, यौगिक के कुल द्रव्यमान की गणना करना संभव है। यह संख्या प्रतिशत द्रव्यमान समीकरण का हर होगा।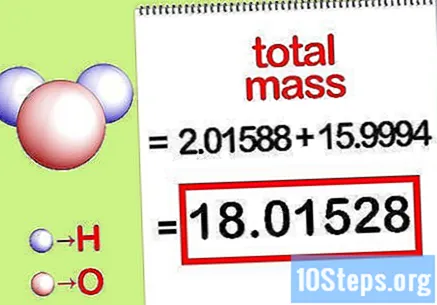
- उदाहरण के लिए, 15.9994 ग्राम / मोल (एक ऑक्सीजन परमाणु के एक एकल तिल का द्रव्यमान) के साथ 2.01588 जी / मोल (हाइड्रोजन परमाणुओं के दो मोल का द्रव्यमान) जोड़ें और 18.01528 ग्राम / मोल प्राप्त करें।
प्रश्न में तत्व के द्रव्यमान को पहचानें। जब आप को खोजने की जरूरत है प्रतिशत द्रव्यमानसमस्या यह है कि आप सभी तत्वों के कुल द्रव्यमान के प्रतिशत के रूप में एक विशिष्ट तत्व के द्रव्यमान को एक यौगिक में ढूंढना चाहते हैं। प्रश्न में तत्व के द्रव्यमान को पहचानें और इसे लिखें। यह दाढ़ अनुपात का उपयोग करके गणना की गई जन मान है। यह मान प्रतिशत द्रव्यमान समीकरण का अंश है।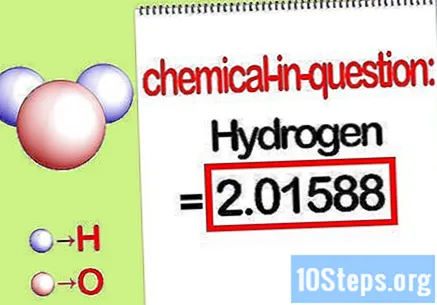
- उदाहरण के लिए, यौगिक का हाइड्रोजन द्रव्यमान 2.01588 ग्राम / मोल (हाइड्रोजन परमाणुओं के दो मोल का द्रव्यमान) है।
- प्रतिशत द्रव्यमान सूत्र में चर को प्रतिस्थापित करें। प्रत्येक चर के लिए मान निर्धारित करने के बाद, उन्हें पहले चरण में परिभाषित समीकरण में प्रतिस्थापित करें: प्रतिशत द्रव्यमान = () x 100।
- उदाहरण के लिए: प्रतिशत द्रव्यमान = () x 100 = () x 100।
प्रतिशत द्रव्यमान की गणना करें। अब जब समीकरण बनता है, तो इसे हल करें ताकि प्रतिशत द्रव्यमान की गणना की जा सके। यौगिक के कुल द्रव्यमान से तत्व के द्रव्यमान को विभाजित करें और 100 से गुणा करें। परिणाम रासायनिक तत्व का प्रतिशत द्रव्यमान होगा।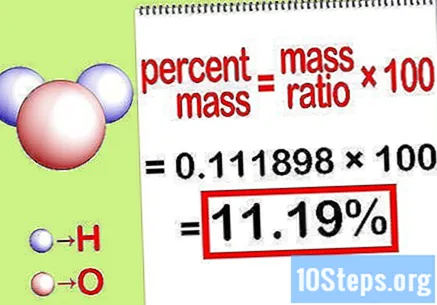
- उदाहरण के लिए, प्रतिशत द्रव्यमान = () x 100 = 0.111189 x 100 = 11.18%। इस प्रकार, पानी के अणु में हाइड्रोजन परमाणुओं का प्रतिशत द्रव्यमान 11.18% है।