
विषय
अन्य खंडरसायन विज्ञान में, अणु की संयोजन क्षमता वे इलेक्ट्रॉन होते हैं जो किसी तत्व के सबसे बाहरी इलेक्ट्रॉन खोल में स्थित होते हैं। यह जानना कि किसी विशेष परमाणु में वैलेंस इलेक्ट्रॉनों की संख्या का पता लगाना रसायन विज्ञानियों के लिए एक महत्वपूर्ण कौशल है क्योंकि यह जानकारी रासायनिक बांडों के प्रकार को निर्धारित करती है जो इसे बना सकते हैं और इसलिए, तत्व की प्रतिक्रियाशीलता। सौभाग्य से, आपको एक तत्व की वैलेंस इलेक्ट्रॉनों को खोजने की आवश्यकता है जो तत्वों का एक मानक आवर्त सारणी है।
कदम
2 का भाग 1: एक आवर्त सारणी के साथ वैलेंस इलेक्ट्रॉनों का पता लगाना
गैर-संक्रमण धातु
लगता है समय समय पर तत्वो की तालिका. यह एक रंग-कोडित तालिका है जो कई अलग-अलग वर्गों से बनी होती है जो मानव जाति के लिए ज्ञात सभी रासायनिक तत्वों को सूचीबद्ध करती है। आवर्त सारणी से तत्वों के बारे में बहुत सारी जानकारी का पता चलता है - हम इस जानकारी का उपयोग उस परमाणु में वैधता इलेक्ट्रॉनों की संख्या निर्धारित करने के लिए करेंगे जिनकी हम जाँच कर रहे हैं। आप आमतौर पर इन्हें रसायन विज्ञान की पाठ्यपुस्तकों के कवर के अंदर पा सकते हैं। यहां ऑनलाइन एक उत्कृष्ट इंटरैक्टिव टेबल भी उपलब्ध है।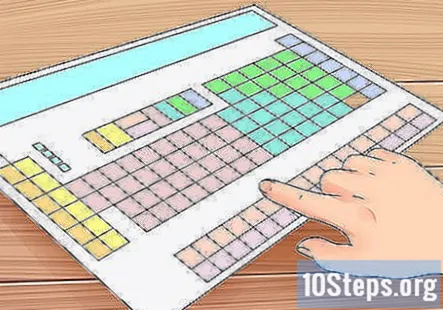

प्रत्येक कॉलम को 1 से 18 तक तत्वों की आवर्त सारणी पर लेबल करें। आम तौर पर, एक आवर्त सारणी पर, एक ही ऊर्ध्वाधर स्तंभ के सभी तत्वों में समान संख्या में वैलेंस इलेक्ट्रॉन होंगे। यदि आपकी आवर्त सारणी में प्रत्येक कॉलम पहले से ही नहीं है, तो प्रत्येक को 1 नंबर से शुरू करें जो कि बाएं छोर के लिए 1 है और 18 सबसे दूर के दाहिने छोर के लिए है। वैज्ञानिक शब्दों में, इन स्तंभों को तत्व कहा जाता है "समूह।"- उदाहरण के लिए, यदि हम एक आवर्त सारणी के साथ काम कर रहे थे, जहाँ समूहों की संख्या नहीं है, तो हम हाइड्रोजन (एच) के ऊपर 1, बेरिलियम (बी) के ऊपर एक 2, और इसी तरह से हीलियम (हे) के ऊपर 18 लिखने तक काम करेंगे। ।
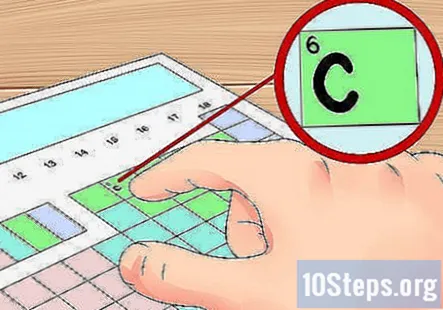
तालिका पर अपना तत्व खोजें। अब, उस तत्व का पता लगाएं, जिसे आप टेबल पर वैलेंस इलेक्ट्रॉनों को खोजना चाहते हैं। आप इसे अपने रासायनिक चिह्न (प्रत्येक बॉक्स में अक्षर), इसका परमाणु क्रमांक (प्रत्येक बॉक्स के शीर्ष बाएं में संख्या), या किसी भी अन्य जानकारी को टेबल पर उपलब्ध करा सकते हैं।- उदाहरण के लिए, आइए एक बहुत ही सामान्य तत्व के लिए वैलेंस इलेक्ट्रॉनों को खोजें: कार्बन (C)। इस तत्व की परमाणु संख्या 6. है। यह समूह 14. के शीर्ष पर स्थित है। अगले चरण में, हम इसकी वैलेंस इलेक्ट्रॉनों को खोज लेंगे।
- इस उपधारा में, हम संक्रमणकालीन धातुओं को अनदेखा करने जा रहे हैं, जो समूह 3 से 12. द्वारा बनाए गए आयताकार आकार के ब्लॉक में तत्व हैं। ये तत्व बाकी हिस्सों से थोड़े अलग हैं, इसलिए इस उपधारा में चरण जीते गए ' उन पर काम नहीं करते। नीचे उपधारा में इनसे कैसे निपटें, यह देखें।
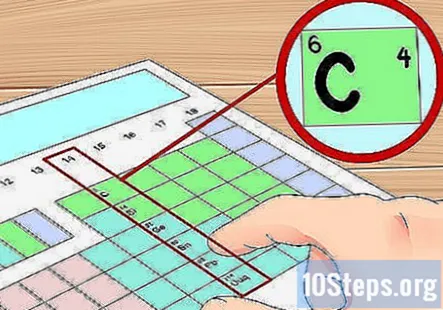
वैलेंस इलेक्ट्रॉनों की संख्या निर्धारित करने के लिए समूह संख्याओं का उपयोग करें। एक गैर-संक्रमण धातु की समूह संख्या का उपयोग उस तत्व के एक परमाणु में वैलेंस इलेक्ट्रॉनों की संख्या को खोजने के लिए किया जा सकता है। समूह संख्या के स्थान इन तत्वों के एक परमाणु में वैलेंस इलेक्ट्रॉनों की संख्या है। दूसरे शब्दों में:- समूह 1: 1 वैलेंस इलेक्ट्रॉन
- समूह 2: 2 वैलेंस इलेक्ट्रॉन
- समूह 13: 3 वैलेंस इलेक्ट्रॉन
- समूह 14: 4 वैलेंस इलेक्ट्रॉन
- समूह 15: 5 वैलेंस इलेक्ट्रॉन
- समूह 16: 6 वैलेंस इलेक्ट्रॉन
- समूह 17: 7 वैलेंस इलेक्ट्रॉन
- समूह 18: 8 वैलेंस इलेक्ट्रॉन (हीलियम को छोड़कर, जिसमें 2 हैं)
- हमारे उदाहरण में, चूंकि कार्बन समूह 14 में है, हम कह सकते हैं कि कार्बन का एक परमाणु है चार वैलेंस इलेक्ट्रॉनों।
संक्रमण धातुओं
समूह 3 से 12 तक एक तत्व का पता लगाएं। जैसा कि ऊपर उल्लेख किया गया है, समूह 3 से 12 के तत्वों को "संक्रमण धातु" कहा जाता है और जब यह वैलेंस इलेक्ट्रॉनों की बात आती है तो बाकी तत्वों की तुलना में अलग व्यवहार करते हैं। इस अनुभाग में, हम यह समझाएंगे कि कैसे, एक निश्चित सीमा तक, इन परमाणुओं को वैलेंस इलेक्ट्रॉनों को निर्दिष्ट करना अक्सर संभव नहीं होता है।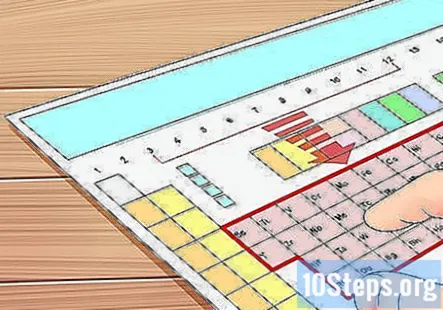
- उदाहरण के प्रयोजनों के लिए, तांतलुम (टा), तत्व 73 को चुनें। अगले कुछ चरणों में, हम इसकी वैलेंस इलेक्ट्रॉनों (या, कम से कम) पाएंगे प्रयत्न सेवा।)
- ध्यान दें कि संक्रमण धातुओं में लैंथेनाइड और एक्टिनाइड श्रृंखला शामिल है (जिसे "दुर्लभ पृथ्वी धातुएं" भी कहा जाता है) - तत्वों की दो पंक्तियां जो आमतौर पर टेबल के बाकी हिस्सों के नीचे स्थित होती हैं जो लैंथेनम और एक्टिनियम से शुरू होती हैं। ये तत्व सभी के हैं समूह ३ आवर्त सारणी का।
समझें कि संक्रमण धातुओं में "पारंपरिक" वैलेंस इलेक्ट्रॉन नहीं हैं। यह समझना कि संक्रमण धातुएँ वास्तव में "काम" क्यों नहीं करती हैं, जैसे कि आवर्त सारणी में इलेक्ट्रॉनों के परमाणुओं में व्यवहार करने के तरीके की थोड़ी व्याख्या की आवश्यकता होती है। त्वरित रन-थ्रू के लिए नीचे देखें या उत्तर के लिए सही होने के लिए इस चरण को छोड़ दें।
- जैसा कि इलेक्ट्रॉनों को एक परमाणु में जोड़ा जाता है, उन्हें अलग-अलग "ऑर्बिटल्स" में विभाजित किया जाता है - मूल रूप से नाभिक के चारों ओर अलग-अलग क्षेत्र जो इलेक्ट्रॉनों में एकत्र होते हैं। आम तौर पर, वैलेंस इलेक्ट्रॉनों सबसे बाहरी शेल में इलेक्ट्रॉन होते हैं - दूसरे शब्दों में, अंतिम इलेक्ट्रॉनों को जोड़ा जाता है। ।
- उन कारणों के लिए जो यहां समझाने के लिए बहुत जटिल हैं, जब इलेक्ट्रॉनों को सबसे बाहरी में जोड़ा जाता है घ एक संक्रमण धातु का खोल (इसके नीचे अधिक), पहले इलेक्ट्रॉन जो शेल में जाते हैं वे सामान्य वैलेंस इलेक्ट्रॉनों की तरह काम करते हैं, लेकिन इसके बाद, वे अन्य कक्षीय परतों से इलेक्ट्रॉनों को नहीं लेते हैं और कभी-कभी वैलेंस इलेक्ट्रॉनों के रूप में कार्य करते हैं। इसका मतलब यह है कि एक परमाणु में वैलेंस इलेक्ट्रॉनों की कई संख्या हो सकती है जो इस बात पर निर्भर करता है कि यह कैसे हेरफेर किया गया है।
समूह संख्या के आधार पर वैलेंस इलेक्ट्रॉनों की संख्या निर्धारित करें। एक बार फिर, जिस तत्व की आप जांच कर रहे हैं उसकी समूह संख्या आपको इसकी वैलेंस इलेक्ट्रॉनों को बता सकती है। हालाँकि, ट्रांज़िशन धातुओं के लिए, ऐसा कोई पैटर्न नहीं है जिसका आप अनुसरण कर सकते हैं - समूह संख्या आमतौर पर वेलेंस इलेक्ट्रॉनों की संभावित संख्या के अनुरूप होगी। य़े हैं: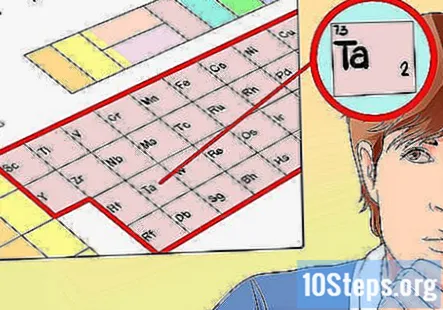
- समूह 3: 3 वैलेंस इलेक्ट्रॉन
- समूह 4: 2 से 4 वैलेंस इलेक्ट्रॉन
- समूह 5: 2 से 5 वैलेंस इलेक्ट्रॉन
- समूह 6: 2 से 6 वैलेंस इलेक्ट्रॉन
- समूह 7: 2 से 7 वैलेंस इलेक्ट्रॉन
- समूह 8: 2 या 3 वैलेंस इलेक्ट्रॉन
- समूह 9: 2 या 3 वैलेंस इलेक्ट्रॉन
- समूह 10: 2 या 3 वैलेंस इलेक्ट्रॉन
- समूह 11: 1 या 2 वैलेंस इलेक्ट्रॉन
- समूह 12: 2 वैलेंस इलेक्ट्रॉन
- हमारे उदाहरण में, चूंकि टैंटलम समूह 5 में है, इसलिए हम कह सकते हैं कि यह बीच में है दो और पांच वैलेंस इलेक्ट्रॉन, दशा पर निर्भर करता है।
भाग 2 का 2: इलेक्ट्रॉन विन्यास के साथ वैलेंस इलेक्ट्रॉनों का पता लगाना
इलेक्ट्रॉन विन्यास पढ़ना सीखें। एक तत्व की वैलेंस इलेक्ट्रॉनों को खोजने का एक और तरीका कुछ है जिसे इलेक्ट्रॉन कॉन्फ़िगरेशन कहा जाता है। ये पहली बार जटिल लग सकते हैं, लेकिन वे अक्षरों और संख्याओं के साथ एक परमाणु में इलेक्ट्रॉन ऑर्बिटल्स का प्रतिनिधित्व करने का एक तरीका नहीं हैं और वे एक बार जब आप जानते हैं कि आप क्या देख रहे हैं, तो वे आसान हैं।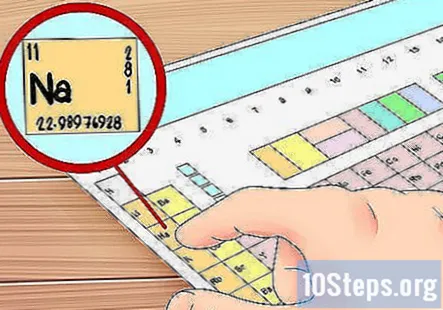
- आइए तत्व सोडियम (Na) के लिए एक उदाहरण विन्यास देखें:
- 1s2s2p3s
- ध्यान दें कि यह इलेक्ट्रॉन विन्यास केवल एक दोहराई जाने वाली स्ट्रिंग है जो इस प्रकार है:
- (संख्या) (पत्र) (संख्या) (पत्र) ...
- ...और इसी तरह। (संख्या) (पत्र) चंक इलेक्ट्रॉन ऑर्बिटल का नाम है और उस ऑर्बिटल में इलेक्ट्रॉनों की संख्या है - यह बात है
- इसलिए, हमारे उदाहरण के लिए, हम कहेंगे कि सोडियम है 1s कक्षीय में 2 इलेक्ट्रॉनों प्लस 2 ऑर्बिटल में 2 इलेक्ट्रॉन प्लस 2p कक्षीय में 6 इलेक्ट्रॉन प्लस 3 एस कक्षीय में 1 इलेक्ट्रॉन। यह कुल 11 इलेक्ट्रॉनों - सोडियम तत्व संख्या 11 है, इसलिए यह समझ में आता है।
- ध्यान रखें कि प्रत्येक उपधारा में एक निश्चित इलेक्ट्रॉन क्षमता होती है। उनकी इलेक्ट्रॉन क्षमता निम्नानुसार है:
- s: 2 इलेक्ट्रॉन क्षमता
- पी: 6 इलेक्ट्रॉन क्षमता
- डी: 10 इलेक्ट्रॉन क्षमता
- एफ: 14 इलेक्ट्रॉन क्षमता
- आइए तत्व सोडियम (Na) के लिए एक उदाहरण विन्यास देखें:
जिस तत्व की आप जांच कर रहे हैं, उसके लिए इलेक्ट्रॉन विन्यास खोजें। एक बार जब आप एक तत्व के इलेक्ट्रॉन विन्यास को जानते हैं, तो इसकी वैलेंस इलेक्ट्रॉनों की संख्या का पता लगाना काफी सरल है (निश्चित रूप से, संक्रमण धातुओं के लिए।) यदि आपको गेट-गो से कॉन्फ़िगरेशन दिया गया है, तो आप अगले चरण पर जा सकते हैं। यदि आपको इसे स्वयं ढूंढना है, तो नीचे देखें:
- ओगनेसन (ओजी), तत्व 118 के लिए पूर्ण इलेक्ट्रॉन विन्यास की जांच करें, जो आवर्त सारणी पर अंतिम तत्व है। इसमें किसी भी तत्व के सबसे अधिक इलेक्ट्रॉन होते हैं, इसलिए इसका इलेक्ट्रॉन विन्यास उन सभी संभावनाओं को प्रदर्शित करता है जिन्हें आप अन्य तत्वों में सामना कर सकते हैं:
- 1s2s2p3s3p4s3d4p5s4d5p6s4f5d6p7s5f6d7p
- अब जब आपके पास यह है, तो आपको केवल एक और परमाणु के इलेक्ट्रॉन विन्यास को खोजने के लिए करने की आवश्यकता है, जब तक कि आप इलेक्ट्रॉनों से बाहर नहीं निकल जाते, तब तक इस पैटर्न को शुरू से ही भरें। यह जितना लगता है उससे कहीं ज्यादा आसान है। उदाहरण के लिए, यदि हम क्लोरीन (Cl), तत्व 17 के लिए कक्षीय आरेख बनाना चाहते हैं, जिसमें 17 इलेक्ट्रॉन हैं, तो हम इसे इस तरह से करेंगे:
- 1s2s2p3s3p
- ध्यान दें कि इलेक्ट्रॉनों की संख्या 17: 2 + 2 + 6 + 2 + 5 = 17 तक जुड़ जाती है। आपको केवल अंतिम ऑर्बिटल में संख्या को बदलने की आवश्यकता है - बाकी वही है क्योंकि ऑर्बिटल्स अंतिम पूर्ण होने से पहले हैं ।
- इलेक्ट्रॉन विन्यास पर अधिक जानकारी के लिए, यह लेख भी देखें।
- ओगनेसन (ओजी), तत्व 118 के लिए पूर्ण इलेक्ट्रॉन विन्यास की जांच करें, जो आवर्त सारणी पर अंतिम तत्व है। इसमें किसी भी तत्व के सबसे अधिक इलेक्ट्रॉन होते हैं, इसलिए इसका इलेक्ट्रॉन विन्यास उन सभी संभावनाओं को प्रदर्शित करता है जिन्हें आप अन्य तत्वों में सामना कर सकते हैं:
ऑक्टेट नियम के साथ कक्षीय गोले को इलेक्ट्रॉनों को असाइन करें। जैसा कि इलेक्ट्रॉनों को एक परमाणु में जोड़ा जाता है, वे ऊपर दिए गए आदेश के अनुसार विभिन्न कक्षाओं में आते हैं - पहले दो 1s कक्षीय में जाते हैं, दो उसके बाद 2s कक्षीय में जाते हैं, छह उसके बाद 2p कक्षीय में जाते हैं, और जल्द ही। जब हम संक्रमण धातुओं के बाहर परमाणुओं के साथ काम कर रहे हैं, तो हम कहते हैं कि ये ऑर्बिटल्स नाभिक के चारों ओर "कक्षीय गोले" बनाते हैं, जिसके प्रत्येक क्रमिक शेल पहले वाले की तुलना में आगे हैं। पहले शेल के अलावा, जो केवल दो इलेक्ट्रॉनों को पकड़ सकता है, प्रत्येक शेल में आठ इलेक्ट्रॉन हो सकते हैं (छोड़कर, फिर से, जब संक्रमण धातुओं के साथ।) इसे कहा जाता है। ओकटेट नियम।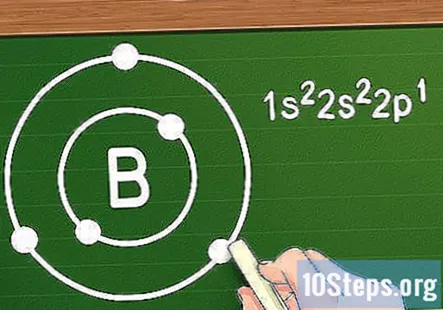
- उदाहरण के लिए, मान लें कि हम बोरॉन (B) तत्व को देख रहे हैं। चूँकि इसकी परमाणु संख्या पाँच है, हम जानते हैं कि इसमें पाँच इलेक्ट्रॉन हैं और इसका इलेक्ट्रॉन विन्यास इस तरह दिखता है: 1s2s2p। चूँकि पहले ऑर्बिटल शेल में केवल दो इलेक्ट्रॉन होते हैं, हम जानते हैं कि बोरोन के दो गोले हैं: एक दो 1s इलेक्ट्रॉनों के साथ और दूसरा 2s और 2p ऑर्बिटल्स वाले तीन इलेक्ट्रॉनों वाला।
- एक अन्य उदाहरण के रूप में, क्लोरीन (1s2s2p3s3p) जैसे तत्व में तीन कक्षीय गोले होंगे: दो 1s इलेक्ट्रॉनों के साथ एक, दो 2s इलेक्ट्रॉनों और छह 2p इलेक्ट्रॉनों के साथ, और एक 3-2 इलेक्ट्रॉनों और पांच 3p इलेक्ट्रॉनों के साथ।
सबसे बाहरी शेल में इलेक्ट्रॉनों की संख्या ज्ञात कीजिए। अब जब आप अपने तत्व के इलेक्ट्रान के गोले को जानते हैं, तो वैलेंस इलेक्ट्रॉनों को खोजना आसान है: केवल सबसे बाहरी शेल में इलेक्ट्रॉनों की संख्या का उपयोग करें। यदि बाहरी शेल भरा हुआ है (दूसरे शब्दों में, यदि इसमें आठ इलेक्ट्रॉन हैं या, पहले शेल के लिए, दो), तो तत्व निष्क्रिय है और अन्य तत्वों के साथ आसानी से प्रतिक्रिया नहीं करेगा। फिर भी, चीजें संक्रमण धातुओं के लिए इन नियमों का काफी पालन नहीं करती हैं।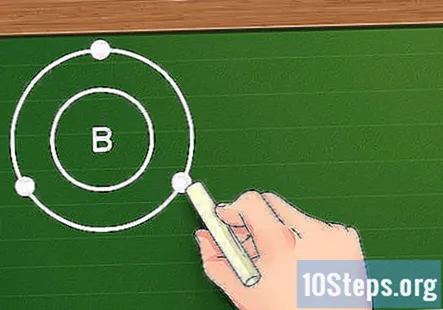
- उदाहरण के लिए, यदि हम बोरोन के साथ काम कर रहे हैं, क्योंकि दूसरे शेल में तीन इलेक्ट्रॉन हैं, तो हम कह सकते हैं कि बोरोन के पास है तीन अणु की संयोजन क्षमता।
कक्षीय शेल शॉर्टकट के रूप में तालिका की पंक्तियों का उपयोग करें। आवर्त सारणी की क्षैतिज पंक्तियों को तत्व कहा जाता है "अवधि।" तालिका के शीर्ष से शुरू करके, प्रत्येक अवधि की संख्या से मेल खाती है इलेक्ट्रॉन के गोले अवधि में परमाणुओं के पास। आप यह निर्धारित करने के लिए एक शॉर्टकट के रूप में उपयोग कर सकते हैं कि किसी तत्व में कितने वैलेंस इलेक्ट्रॉन हैं - बस इलेक्ट्रॉनों की गिनती करते समय इसकी अवधि के बाईं ओर से शुरू करें। एक बार फिर, आप इस पद्धति से संक्रमण धातुओं को अनदेखा करना चाहेंगे, जिसमें समूह 3-12 शामिल हैं।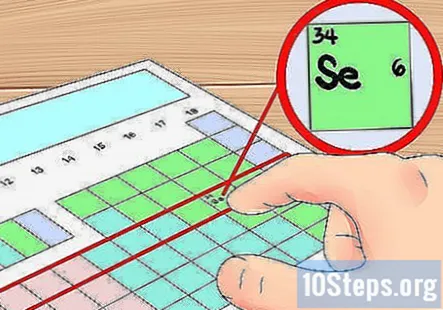
- उदाहरण के लिए, हम जानते हैं कि तत्व सेलेनियम में चार कक्षीय गोले हैं क्योंकि यह चौथी अवधि में है। चूंकि यह चौथी अवधि में बाएं से छठा तत्व है (संक्रमण धातुओं की अनदेखी), हम जानते हैं कि बाहरी चौथे खोल में छह इलेक्ट्रॉन हैं, और इस प्रकार, सेलेनियम है छह वैलेंस इलेक्ट्रॉनों।
सामुदायिक प्रश्न और उत्तर
हम वैलेंस इलेक्ट्रॉन की गणना कैसे करते हैं?
तत्वों के इलेक्ट्रॉनिक कॉन्फ़िगरेशन का निर्धारण करके वैलेंस इलेक्ट्रॉनों को पाया जा सकता है। तत्पश्चात सबसे बाहरी खोल में इलेक्ट्रॉनों की संख्या उस तत्व में कुल वैलेंस इलेक्ट्रॉनों को देती है।
यदि एक परमाणु में 33 इलेक्ट्रॉन होते हैं, तो कितने वैलेंस इलेक्ट्रॉन होते हैं?
यदि परमाणु एक आयन नहीं है, तो हम कह सकते हैं कि परमाणु में 33 प्रोटॉन हैं। इसका मतलब यह तत्व 33 है, जो आर्सेनिक है। तब हम जानते हैं कि यह एक संक्रमण धातु नहीं है, इसलिए हम इसके समूह संख्या 5 की इकाई अंक को देखते हैं और पाते हैं, जिसका अर्थ है कि इसमें 5 वैलेंस इलेक्ट्रॉन हैं।
मैं हीलियम की परमाणु संख्या कैसे निर्धारित करूं?
प्रोटॉनों की संख्या परमाणु संख्या के बराबर होती है।
इलेक्ट्रॉनों को नकारात्मक चार्ज क्यों मिलता है और सकारात्मक चार्ज नहीं?
परमाणु इलेक्ट्रॉनों को प्राप्त या खो देते हैं, नकारात्मक चार्ज करते हैं, क्योंकि प्रोटॉन का सकारात्मक चार्ज होता है और वे नाभिक में मजबूत परमाणु बल द्वारा धारण किए जाते हैं। यह ब्रह्मांड में चार अलग-अलग बलों में से एक है: गुरुत्वाकर्षण, विद्युत चुंबकत्व, कमजोर बल और मजबूत परमाणु बल। यह मजबूत हो गया है क्योंकि प्रोटॉन एक दूसरे को दोहराते हैं फिर भी वे वास्तव में नाभिक में एक साथ बंद होते हैं (न्यूट्रॉन के साथ, जो मजबूत बल द्वारा भी पकड़े जाते हैं।) विचार यह है कि मजबूत बल बेहद मजबूत है लेकिन केवल बहुत छोटी दूरी पर है। छोटे सुपर मजबूत हुक सोचो। प्रोटॉन और न्यूट्रॉन को हुक अप करने के लिए, आपको एक स्टार, सुपरनोवा या परमाणु विस्फोट के विशाल गुरुत्वाकर्षण की तरह बलों की आवश्यकता होती है।
नोबल गैसों की वैलेंस इलेक्ट्रॉन क्या है?
नोबल गैसों में आठ वैलेंस इलेक्ट्रॉन होते हैं - एक तत्व के लिए सबसे स्थिर स्थिति।
नाइट्रोजन में 6 वैलेंस इलेक्ट्रॉन क्यों हैं लेकिन यह समूह 15 में है?
नाइट्रोजन के केवल पांच वैलेंस इलेक्ट्रॉन हैं क्योंकि यह समूह 5 में है, हालांकि यह वास्तव में समूह 15 में है आप संक्रमणकालीन धातुओं को अनदेखा करने जा रहे हैं क्योंकि इन समूहों के पास अपने वैलेंस इलेक्ट्रॉनों को निर्धारित करने का अलग तरीका है। इसलिए: समूह 13 का अर्थ है समूह 3 इत्यादि।
एक परमाणु में 7 प्रोटॉन, 8 न्यूरॉन्स और 7 इलेक्ट्रॉन होते हैं। इसकी वैलेंस शेल में इलेक्ट्रॉनों की संख्या कितनी है?
जिस तत्व में 7 प्रोटॉन होते हैं वह नाइट्रोजन है। नाइट्रोजन उन तत्वों के स्तंभ में है, जिनकी घाटी खोल में 5 इलेक्ट्रॉन हैं। न्यूट्रॉन की संख्या एक विशिष्ट तत्व में वैलेंस इलेक्ट्रॉनों की संख्या को खोजने के लिए अप्रासंगिक है।
आवर्त सारणी पर सात बाहरी शेल इलेक्ट्रॉनों के साथ परमाणु कहाँ स्थित हैं?
निष्क्रिय गैसों के बगल में, दाहिने हाथ की ओर दूसरे से अंतिम कॉलम में देखें।
वैलेंस इलेक्ट्रॉन क्या है?
वैलेंस इलेक्ट्रॉन एक इलेक्ट्रॉन होता है जो परमाणु के सबसे बाहरी भाग पर पाया जाता है और इसे एक प्रतिक्रिया में साझा या लिया जा सकता है।
आवर्त सारणी में तत्वों की वैलेंस इलेक्ट्रॉनों की अलग-अलग संख्या क्यों है?
उनके पास विभिन्न रासायनिक संरचनाएं हैं। वैलेंस इलेक्ट्रॉन रासायनिक प्रतिक्रिया पैदा करते हैं।
टिप्स
- ध्यान दें कि कॉन्फ़िगरेशन की शुरुआत में ऑर्बिटल्स के लिए खड़े होने के लिए रईस गैंडों (समूह 18 में तत्वों) का उपयोग करके इलेक्ट्रॉन विन्यास को शॉर्टहैंड के एक प्रकार में लिखा जा सकता है। उदाहरण के लिए, सोडियम के इलेक्ट्रॉन विन्यास को 3s1 लिखा जा सकता है - अनिवार्य रूप से, यह नियॉन के समान है, लेकिन 3s कक्ष में एक और इलेक्ट्रॉन के साथ।
- संक्रमण धातुओं में वैलेंस सबशेल हो सकते हैं जो पूरी तरह से भरे हुए नहीं हैं। संक्रमण धातुओं में वैलेंस इलेक्ट्रॉनों की सटीक संख्या निर्धारित करने में क्वांटम सिद्धांत के सिद्धांत शामिल हैं जो इस लेख के दायरे से परे हैं।
- इस बात पर ध्यान दें कि समय-समय पर तालिकाएँ देश से भिन्न होती हैं। इसलिए, कृपया जांचें कि आप भ्रम से बचने के लिए सही, अपडेट किए गए का उपयोग कर रहे हैं।
- वैलेंस इलेक्ट्रॉनों को खोजने के लिए अंतिम कक्षीय से जोड़ना या घटाना सुनिश्चित करना सुनिश्चित करें।
चीजें आप की आवश्यकता होगी
- समय समय पर तत्वो की तालिका
- पेंसिल
- कागज़
WikiHow में हर दिन, हम आपको ऐसे निर्देशों और सूचनाओं तक पहुँच प्रदान करने के लिए कड़ी मेहनत करते हैं जो आपको एक बेहतर जीवन जीने में मदद करेंगे, चाहे वह आपको सुरक्षित रखे, स्वस्थ हो, या आपकी भलाई में सुधार करे। वर्तमान सार्वजनिक स्वास्थ्य और आर्थिक संकटों के बीच, जब दुनिया नाटकीय रूप से बदल रही है और हम सभी दैनिक जीवन में बदलावों के बारे में सीख रहे हैं और अपना रहे हैं, लोगों को पहले से कहीं ज्यादा विकी की जरूरत है। आपका समर्थन wikiHow को अधिक गहराई से सचित्र लेख और वीडियो बनाने और हमारे विश्वसनीय ब्रांड को दुनिया भर के लाखों लोगों के साथ साझा करने में मदद करता है। कृपया आज विकि को योगदान देने पर विचार करें।


